ბორიუმი
| ბორიუმი |
| 107Bh |
| [270] |
| 5f14 6d5 7s2 |
ბორიუმი[1] (ლათ. Bohrium; ქიმიური სიმბოლო — ), უნნილსეპტიუმი (ლათ. Unnilseptium; ქიმიური სიმბოლო — ), ეკა-რენიუმი (Eka-rhenium) — ელემენტთა პერიოდული სისტემის მეშვიდე პერიოდის, მეშვიდე ჯგუფის (მოძველებული კლასიფიკაციით — მეშვიდე ჯგუფის თანაური ქვეჯგუფის, VIIბ) ხელოვნურად მიღებული რადიოაქტიური ქიმიური ელემენტი. მისი ატომური ნომერია — 107. ცნობილია იზოტოპები, რომელთა მასური რიცხვია 261-დან 272. მიღებული იზოტოპებიდან ყველაზე სტაბილური იზოტოპია — ბორიუმ-267 რომლის ნახევარდაშლის პერიოდია 17 წმ[2]. ელემენტს სახელი დაერქვა დანიელი ფიზიკოსის ნილს ბორის პატივსაცემად.
| ზოგადი თვისებები | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| მასური რიცხვი | 270 | |||||||||||||||||||||||||||||||||||
| ბორიუმი პერიოდულ სისტემაში | ||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||
| ატომური ნომერი (Z) | 107 | |||||||||||||||||||||||||||||||||||
| ჯგუფი | 7 | |||||||||||||||||||||||||||||||||||
| პერიოდი | 7 პერიოდი | |||||||||||||||||||||||||||||||||||
| ბლოკი |
| |||||||||||||||||||||||||||||||||||
| ელექტრონული კონფიგურაცია | [Rn] 5f14 6d5 7s2 | |||||||||||||||||||||||||||||||||||
| ელექტრონი გარსზე | 2, 8, 18, 32, 32, 12, 2 | |||||||||||||||||||||||||||||||||||
ელემენტის ატომის სქემა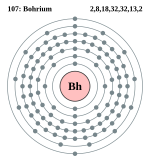 | ||||||||||||||||||||||||||||||||||||
| ფიზიკური თვისებები | ||||||||||||||||||||||||||||||||||||
| აგრეგეგატული მდგომ. ნსპ-ში | მყარი სხეული | |||||||||||||||||||||||||||||||||||
| სიმკვრივე (ო.ტ.) | 26–27 გ/სმ3 | |||||||||||||||||||||||||||||||||||
| ატომის თვისებები | ||||||||||||||||||||||||||||||||||||
| ჟანგვის ხარისხი | (+3), (+4), (+5), +7 | |||||||||||||||||||||||||||||||||||
| ელექტროდული პოტენციალი |
| |||||||||||||||||||||||||||||||||||
| იონიზაციის ენერგია |
| |||||||||||||||||||||||||||||||||||
| ატომის რადიუსი | ემპირიული: 128 პმ | |||||||||||||||||||||||||||||||||||
| კოვალენტური რადიუსი (rcov) | 141 პმ | |||||||||||||||||||||||||||||||||||
| სხვა თვისებები | ||||||||||||||||||||||||||||||||||||
| ბუნებაში გვხვდება | სინთეზირების შედეგად | |||||||||||||||||||||||||||||||||||
| მესრის სტრუქტურა |
მჭიდრო ჰექსაგონალური | |||||||||||||||||||||||||||||||||||
| CAS ნომერი | 54037-14-8 | |||||||||||||||||||||||||||||||||||
| ისტორია | ||||||||||||||||||||||||||||||||||||
| სახელწოდება მომდინარეობს | ნილს ბორის გვარის მიხედვით | |||||||||||||||||||||||||||||||||||
| აღმომჩენია | Gesellschaft für Schwerionenforschung (1981) | |||||||||||||||||||||||||||||||||||
| ბორიუმის მთავარი იზოტოპები | ||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||
| • | ||||||||||||||||||||||||||||||||||||
ისტორია
რედაქტირება1976 წელს 107-ე ელემენტის სინთეზის შესახებ პირველი განაცხადა იური ოგანესიანის ჯგუფმა დუბნიდან[3]. ამ ნამუშევარის მეთოდიკა მდგომარეობდა - ბისმუტ-209-ისა და ქრომ-54-ის ბირთვების შერწყმის რეაქციის სპონტანური დაყოფის პროდუქტების კვლევაში. ნაპოვნი იქნა ორი დამახასიათებელი ნახევარდაშლის დრო: 5 წმ. და 1—2 მლწმ. პირველი მიწერილი იყო ბირთვ 257105-ის დაშლაზე, რადგანაც ასეთივე ნახევარდაშლის პერიოდი იყო 105-ე ელემენტის მიღების რეაქციის პროდუქტებისათვის: 209Bi+50Ti, 208Pb+51V, 205Tl+54Cr. ნახევარდაშლის მეორე პერიოდი მიეწერა ბირთვს 261107, რომელსაც, მეცნიერების ვარაუდით, აქვს ორი დაშლა: სპონტანური დაშლა (20 %) და α-დაშლა, რომელიც იწვევს წარმოქმნილი ბირთვის 257105 სპონტანურ დაშლას ნახევარდაშლის პერიოდით 5 წმ.
1981 წელს გერმანელი მეცნიერების ჯგუფმა დარმშტადტის მძიმე იონების ინსტიტუტიდან (გერმ. Gesellschaft für Schwerionenforschung, GSI) გამოიკვლია იგივე რეაქციის პროდუქტები 209Bi+54Cr, და გამოიყენა უფრო დახვეწილი მეთოდიკა, რომელიც იძლეოდა საშუალებას აღმოეჩინა ნუკლიდების α-დაშლა და განესაზღვრათ მისი პარამეტრები. თავის ექსპერიმენტში GSI -ის მეცნიერებმა მოახდინეს ბირთვ 262107-ის α-დაშლის 5 მოვლენის იდენტიფიცირება, და მათი სიცოცხლის დრო შეაფასეს 4,7+2,3−1,6 წმ[4].
როგორც 107, 105 და 104 ელემენტების იზოტოპების შემდგომ კვლევამ აჩვენა, რეაქციაში 209Bi+54Cr მართლაც იბადება, ჩნდება ბირთვები 261107 და 262107[5]. მაგრამ 1976 წელს დუბნის მენიერების მიერ მიღებული ბევრი დასკნა გამოვიდა მცდარი. კერძოდ, ნახევარდაშლის პერიოდი 5 წმ ააქვს არა 257105, არამედ 258105[6]. 1/3 ალბათობით ეს ნუკლიდი განიცდის ბეტა-დაშლას და გარდაიქმნება 258104-ში, რომელიც ძალიან ჩქარა (ნახევარდაშლის პერიოდი 12 მლწმ) იყოფა სპონტანურად. ეს ნიშნავს, რომ დუბნის ჯგუფი აკვირდებოდნენ არა ბირთვ 262107-ის α-დაშლის პროდუქტებს, არამედ 261107[7]. იზოტოპ 261107-ის სიცოცხლის დრო თანამედროვე მონაცემებით შეადგენს 12 მლწმ., რაც შედარებით მეტია ვიდრე 1976 წელს დამტკიცებული დრო.
სახელწოდება
რედაქტირება1992 წლის სექტემბერში დარმშტადტის და დუბნის მეცნიერებს შორის მიღწეულ იქნა შეთანხმება იმის შესახებ, რომ 107 ელემენტს ეწოდოს «ნილსბორიუმი» დანიელი ფიზიკოსის ნილს ბორის პატივსაცემად[8], თუმცა თავდაპირველად საბჭოთა მეცნიერები გეგმავდნენ «ნილსბორიუმი» 105-ე ელემენტისათვის ეწოდებინათ (ახლა ეს ელემენტი დუბნიუმია)[7]. 1993 წელს IUPAC-მა აღიარა გერმანელი მეცნიერების პრიორიტეტი 107-ე ელემენტის იდენტიფიკაციაში[7], და 1994 წელს თავის რეკომენდაციაში წარმოადგინა სახელწოდება «ბორიუმი», რადგანაც ქიმიური ელემენტების სახელცოდებები არასდროს არ შედგებოდა მეცნიერის სახელი გვარისაგან[9]. ეს გადაწყვეტილება საბოლოოდ მიღებული იქნა 1997 წელს დანიელი ქიმიკოსებთან კონსულტაციის შემდეგ[10].
ცნობილი იზოტოპები
რედაქტირება| იზოტოპი | მასა | ნახევარდაშლის პერიოდი[11] | დაშლის ტიპი |
|---|---|---|---|
| 261Bh | 261 | 12თარგი:Sup sub მლწმ | α-დაშლა 257Db |
| 262Bh | 262 | 8,0±2,1 мс | α-დაშლა 258Db |
| 264Bh | 264 | წმ | α-დაშლა 260Db |
| 265Bh | 265 | წმ | α-დაშლა 261Db |
| 266Bh | 266 | წმ | α-დაშლა 262Db |
| 267Bh | 267 | წმ | α-დაშლა263Db |
| 272Bh | 272 | წმ | α-დაშლა268Db |
რესურსები ინტერნეტში
რედაქტირება- ბორიუმი Webelements-ზე
- ბორიუმი ქიმიური ელემენტების პოპულარულ ბიბლიოთეკაში დაარქივებული 2018-12-03 საიტზე Wayback Machine.
- WebElements.com — Bohrium
- EnvironmentalChemistry.com — Bohrium
- Los Alamos National Laboratory — Bohrium დაარქივებული 2010-12-12 საიტზე Wayback Machine.
- ელემენტის სინთეზის შესახებ საიტზე ОИЯИ დაარქივებული 2018-12-25 საიტზე Wayback Machine.
სქოლიო
რედაქტირება- ↑ ბორიუმი — ტექნიკური ლექსიკონი
- ↑ Evidence for New Isotopes of Element 107: 266Bh and 267Bh, Physical Review Letters, 2000, ტ. 85, № 13, გვ. 2697 - 2700.
- ↑ Yu. Ts. Oganessian et al., On spontaneous fission of neutron-deficient isotopes of elements 103, 105 and 107, Nuclear Physics A, 1976, ტ. 273, № 2, გვ. 505-522.
- ↑ G. Münzenberg et al., Identification of element 107 by α correlation chains, Zeitschrift für Physik A, 1981, ტ. 300, № 1, გვ. 107-108.
- ↑ G. Münzenberg et al., Element 107, Zeitschrift für Physik A, 1989, ტ. 333, № 2, გვ. 163-175.
- ↑ The new isotopes 258105, 257105, 254Lr and 253Lr, Zeitschrift für Physik A, 1985, ტ. 322, № 4, გვ. 557-566.
- ↑ 7.0 7.1 7.2 R. C. Barber et al., Discovery of the transfermium elements, Pure and Applied Chemistry, 1993, ტ. 65, № 8, გვ. 1757-1814.
- ↑ Responses on the Report 'Discovery of the transfermium elements', Pure and Applied Chemistry, 1993, ტ. 65, № 8, გვ. 1815-1824.
- ↑ Commission on Nomenclature of Inorganic Chemistry, Names and symbols of transfermium elements (IUPAC Recommendations 1994), Pure and Applied Chemistry, 1994, ტ. 66, № 12, გვ. 2419-2421.
- ↑ Commission on Nomenclature of Inorganic Chemistry, Names and symbols of transfermium elements (IUPAC Recommendations 1997), Pure and Applied Chemistry, 1997, ტ. 69, № 12, გვ. 2471-2473.
- ↑ Nudat 2.3


