ამიაკი
ქიმიური ნივთიერება
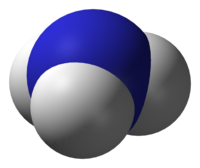
ამიაკი — ქიმიური ნივთიერება, მისი ფორმულაა NH3. ნორმალურ პირობებში (ნ.პ.) უფერო აირია, მკვეთრი დამახასიათებელი სუნით. ამიაკის სიმკვრივე თითქმის ორჯერ ნაკლებია ჰაერისაზე.
| ამიაკი | |
 | |
 | |
| ზოგადი | |
|---|---|
| სისტემური სახელწოდება | ამიაკი |
| ქიმიური ფორმულა | NH3 |
| მოლური მასა | 17.031 გ/მოლი |
| თერმული თვისებები | |
| დნობის ტემპერატურა | −77.73 °C |
| დუღილის ტემპერატურა | −33.34 °C |
| სტრუქტურა | |
| დიპოლური მომენტი | 1.42 დ |
| კლასიფიკაცია | |
| CAS | 7664-41-7 |
| PubChem | 222 |
| SMILES |
|
| RTECS | BO0875000 |
ამიაკის ერთი მოლეკულა სამკუთხა პირამიდას წარმოადგენს, რომლის წვერშიც აზოტი მდებარეობს.
ამიაკის მოლეკულები −77.73°C ტემპერატურაზე დნობას, ხოლო −33.34°C დუღილს იწყებენ.
2014 წელს გლობალურ ინდუსტრიაში 176 300 000 ტონა [1] ამიაკი აწარმოეს, რაც 16%-ით მეტია 2006 წლის მაჩვენებელზე (152 000 000 ტონა[2]).
ამიაკი სუფთა სახით 1774 წელს ჯოზეფ პრისტლიმ აღმოაჩინა და „ტუტე ჰაერი“ (ინგლ. alkaline air) უწოდა[3]. 11 წლის შემდეგ კი 1785 წელს კლოდ ლუი ბერტოლმა მისი ზუსტი ქიმიური შედგენილობა დაადგინა.[4]
ლიტერატურა
რედაქტირება- (1986) რედ. Bretherick, L.: Hazards in the Chemical Laboratory, 4th, London: Royal Society of Chemistry. ISBN 0-85186-489-9. OCLC 16985764.
რესურსები ინტერნეტში
რედაქტირებავიკისაწყობში არის გვერდი თემაზე:
- ამიაკი, უცხო სიტყვათა ლექსიკონი www.nplg.gov.ge
- International Chemical Safety Card 0414 (anhydrous ammonia), ilo.org.
- International Chemical Safety Card 0215 (aqueous solutions), ilo.org.
- Ammoniac et solutions aqueuses fr. Institut National de Recherche et de Sécurité. დაარქივებულია ორიგინალიდან — 2010-12-11. ციტირების თარიღი: 2016-07-22.
- Emergency Response to Ammonia Fertilizer Releases (Spills) for the Minnesota Department of Agriculture.ammoniaspills.org
- National Institute for Occupational Safety and Health – Ammonia Page, cdc.gov
- NIOSH Pocket Guide to Chemical Hazards - Ammonia, cdc.gov
- Ammonia, video დაარქივებული 2015-10-30 საიტზე Wayback Machine.
სქოლიო
რედაქტირება- ↑ pg. 119 – Nitrogen (PDF). USGS (2016). ციტირების თარიღი: 17 February 2016.
- ↑ Nitrogen (PDF). USGS (2016). ციტირების თარიღი: 17 February 2016.
- ↑ Priestley, Joseph (1775). „Observations on Alkaline Air“, Experiments and Observations on Different Kinds of Air, Second edition, გვ. 163-177.
- ↑ Berthollet (1788). „Analyse de'l Alkali volatil“. Histoire de l'Académie Royale des Sciences. Année M. DCCLXXXV. Avec les Mémoires de Mathématique & de Physique pour la même Année: 316–326.